6. Влияние
легирующих элементов на полиморфизм железа. Классификация сталей по структуре
отжига.
Влияние элементов на
полиморфизм железа
Расширение g-области
элементами, образующими твердые растворы внедрения, объясняется большей их
растворимостью в ГКЦ решетке, а расширение g-области при образовании
твердых растворов замещения –близостью их кристаллического строения аустениту.
Такие элементы могут расширить g-область до
комнатных и более низких температур. Стали со стабильной аустенитной структурой во всем температурном интервале
вплоть до плавления называются аустенитными.

Если области a-и d-растворов смыкаются, то структура с ОЦК решеткой стабильна во всем интервале температур. Такие стали называются ферритными.
Четкого объяснения влияния л.э. на полиморфизм железа нет. Подмечено только, что элементы с атомным радиусом больше, чем у Fe-, сужают g-область.
Свыше определённого содержания
марганца, никеля и других элементов, имеющих гранецентрированную кубическую
решетку, – состояние существует как стабильное от комнатной температуры до
температуры плавления, такие сплавы на основе железа называются аустенитными. При содержании ванадия, молибдена, кремния и
других элементов, имеющих объемно-центрированную кубическую решетку. Выше
определённого предела устойчивым при всех температурах является α– состояние. Такие сплавы на основе железа называются
ферритными. Аустенитные и ферритные сплавы не имеют
превращений при нагреве и охлаждении.
Классификация сталей по равновесной структуре отжига
1. Стали доэвтектоидные;
2. -----«----- эвтектоидные;
3. -----«----- заэвтектоидные;
4. -----«-----ледебуритные;
5. -----«-----ферритные нет a®g;
6. -----«-----аустенитные нет a®g;
7. -----«-----полуферритные частичное a® g превращение.
7. Влияние
легирующих элементов на растворимость углерода в аустените, температуру
эвтектоидного превращения, устойчивость переохлажденного аустенита.
Классификация сталей по структуре
нормализации.
Подавляющее количество л.э. уменьшают растворимость углерода в аустените и концентрацию углерода в эвтектоидной стали, т.е. сдвигают точки E и S влево (исключение – сильные карбидообразователи типа V и Ti); элементы, расширяющие g-область снижают температуру А1(например, Ni, Mn); элементы, сужающие g-область – повышают температуру А1 (например, Cr, Si).
Все легирующие элементы превращают температуры эвтектического и эвтектоидного превращения в интервал температур в соответствие с правилом фаз Гиббса.
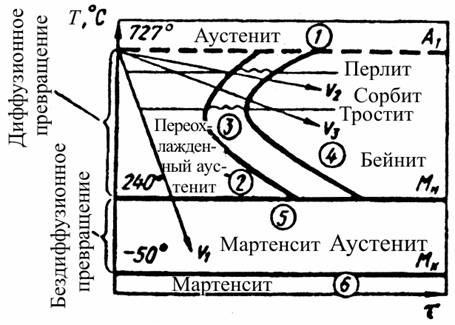
Диаграмма изотермического превращения аустенита эвтектоидной стали.
На диаграмме можно выделить следующие области: 1) область устойчивого аустенита (для стали, содержащей 0,8 % С, выше АС1); 2) область переохлажденного аустенита; 3) область начавшегося, но еще не закончившегося превращения А => П; 4) область закончившегося превращения А => П; 5) область начавшегося, но еще не закончившегося мартенситного превращения (между Мн–Mк); 6) мартенситная область (ниже Мк).
Область, расположенная слева от кривой начала распада аустенита (область переохлажденного аустенита), определяет продолжительность инкубационного периода, характеризующую устойчивость переохлажденного аустенита. С увеличением переохлаждения его устойчивость быстро уменьшается, достигая минимума (для эвтектоидной стали около 550 °С), и далее вновь возрастает.
В зависимости от степени переохлаждения аустенита различают три температурные области превращения: перлитную (переохлаждение до 500 °С), мартенситную (переохлаждение ниже Мн — для эвтектоидной стали ниже температуры 240 °С) и промежуточного (бейнитного) превращения (переохлаждение для эвтектоидной стали в интервале от 500 до 240 °С).
По структурам после нормализации различают следующие классы легированных сталей: перлитный М+Ф, мартенситный а+М, аустенитный а+Ф (в интернете еще пишут,что ферритный и ледебуритный).
8.
Хромистые, никелевые и хромоникелевые стали. Структурные диаграммы легированных
сталей.
Никелевые
стали.
Особенностью
сплавов Fe-Ni с высоким содержанием никеля является
медленный распад аустенита при низких температурах. Об этом свидетельствует наличие по крайней мере трёх разных диаграмм состояния Fe-Ni.
Наиболее
часто приводится диаграмма (рис.1) . Равновесие в области α+γ достигается при выдержках до двух
лет.

При
содержании Ni от 5 до 35 % при охлаждении на
воздухе γ→α
превращение идёт по мартенситному механизму, при медленном нагреве превращение α→γ+α осуществляется диффузионным путём. При быстром
нагреве возможно α'+γ
превращение как обратное мартенситное и только потом гетерогенный распад на α+γ-фазы: α'→γ'→α+γ
Ni- один из
полезнейших легирующих элементов сталей, повышающий их прокаливаемость,
прочность, запас вязкости одновременно. В этом отношении Ni-
восьмое чудо света. Ni- основной
легирующий элемент хладостойких и жаропрочных сталей.
Система
Fe-Ni - основа сплавов с особыми физическими свойствами: инварные сплавы, элинварные
сплавы, например 36Н(36%Ni,
Fe-ост), 32HKD (32%Ni, 4%Co, 1%Cu) суперинвар,
44НХТЮ( 44%Ni,
5%Cr, 2,5%Ti, 0,7%Al) элинвар и т.д..
Особенности
аустенитных сталей с высоким содержанием Ni является наличие двойников в структуре после закалки и отжига (рис. 4).
Введение
никеля в стали (Fe+C)
приводит к смещению точки S влево и вниз, а
точки E - влево и
вверх, т.е. содержание углерода в эвтектоиде уменьшается,
точка А3 понижается, а точка Аст
- повышается. Так при 5% никеля точка S соответствует
650° С и 0,2% С.
Хромистые
стали.
Хром пожалуй самый распространнённый
легирующий элемент сталей. Он повышает прочность, износостойкость, прокаливаемость, при содержании более 13% делает сталь коррозионностойкой.

σ фаза - электронное соединение с
концентрацией валентных электронов равной 7. Решетка - слоистая тетрагональная
С30 (аналог β-уран). Ее образование в сплавах ведет к потере
пластичности.
В
сталях в зависимости от содержания Cr и С присутствуют 3 типа карбидных фаз (Fe,Cr)
Особенности
фазовых превращений сплавов Fe-Cr-C определяются тем, что С расширяет, а Cr сужает γ-область. Поэтому в зависимости от содержания Cr и С могут
быть стали: при 0,5% С с повышением содержания Cr доэвтектоидные, заэвтектоидные, ледебуритные, полуферритные, ферритные.
Микросруктура хромистых сталей с высоким
содержанием С –более тёмная матрица+
карбиды. Причём ее вид практически одинаков после закалки или отжига.
Сложно-легированные Cr-Ni стали.
Изобразить
в пространстве д.с. Fe-Cr-Ni уже невозможно. А промышленные стали
содержат (всегда!) и другие элементы. Поэтому на практике пользуются так
называемыми структурными диаграммами. При этом учитывают, что л.э. действуют
или как Cr(т.е.
сужают γ-область), или как Ni (расширяют ее) с разной интенсивностью.
Подсчитывается
как бы приведённое содержание Cr
и Ni. Интенсивность
влияния л.э. учитывается введением коэффициентов,
определяемых на основании опыта.
Crэкв=ECr=Cr + 2Si + 1,5Mo +
5V + 5,5Al + 1,75Nb + 1,5Ti + 0,75W
Niэкв=ENi=Ni + 0,5Mn +
Построенные
таким образом диаграммы (структурные) справедливы для определенного состояния
(рис.8).

Очень
часто определяемые по таким диаграммам структуры являются метастабильными и при
других обработках меняют свою структуру.
Например,
сталь 08*18Н9- сталь аустенитного класса. Такую
структуру она имеет в литом и закалённом состоянии. Уже при наклёпе (например,
прокатке при комнатной температуре) появляется α-фаза по мартенситному
механизму- мартенсит деформации.
9. Структуры
отожженных, нормализованных и закаленных сталей.

Структура, образующаяся при непрерывном охлаждении стали, может быть предсказана на основе анализа С-диаграммы. Если эвтектоидную сталь нагреть до температуры выше АС1, при которой она полностью приобретает структуру аустенита, а затем охладить до комнатной температуры, то получится структура, зависящая от скорости охлаждения. При малой скорости V1 продолжительность пребывания углеродистой стали при высокой температуре (несколько ниже АС1) такова, что распад аустенита завершается образованием крупно-пластинчатого перлита. Такой процесс называется отжигом. Практически он осуществляется путем охлаждения стали в печи с большой тепловой инерцией, что приводит к получению сравнительно малой твердости отжигаемой стали. Скорость охлаждения равна по порядку величины 0,1 К/с. На рис. 240 на кривой v1 показано замедление охлаждения в области распада, которое обусловлено выделением тепла при превращении аустенит>перлит. В случае V2>V1 превращение начинается при более низкой температуре и приводит к получению тонкопластинчатого перлита с большей твердостью. На практике для получения такой структуры часто охлаждение ведут на воздухе со скоростью порядка 1 К/с. Такая обработка называется нормализацией. Можно представить себе скорость охлаждения V3 (> V2), при которой только часть аустенита распадается и образуется тонкопластинчатый перлит. В этом случае оставшийся аустенит, охладившись ниже точки МН (230 °С), превратится в мартенсит. Сохранится и небольшое количество остаточного аустенита. На кривой V3 получается замедление охлаждения в двух температурных интервалах, в которых образуются соответственно перлит и большая часть мартенсита (близко к 230 °С). При скорости V4>V3, как видно из рис. 240, распад аустенита практически не начинается и аустенит только превращается и мартенсит. Остается некоторое количество остаточного аустенита. Такая операция называется закалкой стали.
10.
Диаграммы железо - углерод и железо - графит. Факторы, стабилизирующие цементит
и графит.



Если в равновесии с жидкой фазой, аустенитом и ферритом находится графит, то равновесие является стабильным. В случае, когда и равновесии с этими фазами, т. е. растворами на базе железа, находится цементит, равновесие является метастабильным. В обоих случаях равновесию любого сплава Fe—C заданного состава соответствует минимум термодинамического потенциала, но его минимальное значение в случае стабильного равновесия меньше, чем в случае метастабильного равновесия. На рис. 203 схематически показано изменение свободной энергии в стабильной и метастабильной системе в функции содержания углерода при высокой температуре, при которой в равновесии находится аустенит. Видно, что уменьшение свободной энергии (ΔF) должно приводить к распаду цементита (графитизации). Видно также, что содержание углерода в аустените в стабильной системе (С') ниже, чем в метастабильной (С). Сказанное относится и к равновесию феррита с графитом или цементитом.